Bayangkan sebuah pasir hitam yang biasa terhampar di pantai, seperti yang ada di Pulau Bangka, Indonesia, atau di Pulmoddai, Sri Lanka. Tampilannya mungkin biasa saja, tetapi di dalamnya tersembunyi harta karun industri modern yaitu ilmenit. Mineral dengan rumus kimia FeTiO₃ ini adalah cikal bakal terciptanya titanium dioksida (TiO₂), senyawa serba guna yang menjadi tulang punggung industri cat, kertas, plastik, kosmetik, dan bahkan teknologi pemurnian air dan energi surya (Sampath et al., 2023). Namun, mengubah bongkahan ilmenit yang “keras kepala” menjadi produk titanium yang bernilai tinggi bukanlah proses yang mudah. Dunia ilmu pengetahuan dan industri telah lama mencari metode yang paling efisien, ekonomis, dan ramah lingkungan untuk mewujudkannya.
Dua Raksasa Proses Industri: Proses Sulfat vs. Klorida
Secara global, proses sulfat dan proses klorida mendominasi sebagai metode produksi TiO2 dari ilmenit.
- Proses Sulfat : Si Lama dan Tangguh
Proses sulfat dilakukan dengan mengandalkan asam sulfat pekat (H₂SO₄) untuk “melarutkan” ilmenit. Proses ini terdiri dari empat tahapan : pencernaan asam, hidrolisis, kalsinasi, dan perlakuan akhir. Keunggulan utama proses ini adalah kemampuannya menghasilkan TiO₂ dalam dua fase kristal yang diinginkan industri, yaitu anatase atau rutile, hanya dengan mengatur suhu kalsinasi (Sampath et al., 2023). Selain itu, biaya investasi dan operasinya relatif lebih murah. Namun, proses ini menyisakan bayangan gelap bagi lingkungan. Untuk setiap ton TiO₂ yang dihasilkan, proses ini menghasilkan hingga 11 ton asam bekas, 200 ton air asam, dan 25.000 m³ gas buang (Sampath et al., 2023).
- Proses Klorida: Si Modern yang Eksklusif
Berbeda dengan sebelumnya, proses klorida adalah proses kontinu yang lebih modern. Metode ini menggunakan gas klorin (Cl₂) untuk mengubah bijih rutile berkadar tinggi menjadi titanium tetraklorida (TiCl₄), yang kemudian dibakar dengan oksigen untuk menghasilkan TiO₂. Proses ini menghasilkan TiO₂ rutile dengan kemurnian sangat tinggi dan limbah yang lebih sedikit, karena gas klorin dapat didaur ulang (Sampath et al., 2023). Sayangnya, proses ini sangat eksklusif, karena hanya daapat “memproses” bijih rutile alam atau sintetis berkadar tinggi, yang harganya mahal dan ketersediaannya terbatas. Selain itu, proses ini hanya menghasilkan fase rutile dan membutuhkan kondisi yang sangat kering serta suhu tinggi, sehingga biaya operasionalnya melambung.
Langkah Cerdas: Mengubah Ilmenit Menjadi “Rutile Sintetis”
Keberadaan rutile di alam semakin langka, para ilmuwan menemukan cara cerdas: meningkatkan mutu (upgrading) ilmenit menjadi “rutile sintetis”. Beberapa proses seperti Becher, Laporte, dan Kataoka dikembangkan dengan prinsip yang mirip: pertama-tama, struktur ilmenit diubah melalui pemanasan dengan udara (oksidasi) dan reduksi, lalu besi sebagai pengotor dipisahkan dengan pencucian asam lemah.
Proses Kataoka, misalnya dinilai lebih “hijau” karena beroperasi pada suhu yang lebih rendah dan menggunakan asam dalam konsentrasi rendah, namun tetap mampu memulihkan lebih dari 95% TiO₂ yang terkandung (Sampath et al., 2023).
Inovasi Terkini: Mencari Jalan yang Lebih Hijau dan Beragam
Keterbatasan proses konvensional memicu lahirnya berbagai metode inovatif yang tidak hanya berfokus pada TiO₂, tetapi juga menghasilkan beragam senyawa titanium dan paduan (alloy) yang bernilai.
Dekomposisi Alkali (NaOH/KOH) dan Rute Pemurnian EDTA
Metode ini menawarkan alternatif yang menarik dengan menggunakan basa kuat sebagai jantung prosesnya. Sebuah studi mendemonstrasikan rute produksi TiO₂ yang efisien seperti yang terlihat pada Gambar 1.1
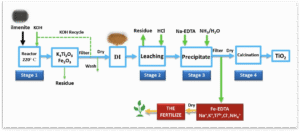 |
Prosesnya dimulai dengan mereaksikan ilmenit dengan Kalium Hidroksida (KOH) pada suhu 220°C (Stage 1), yang mengubah ilmenit menjadi kalium titanat (K₄Ti₃O₈) dan oksida besi (Fe₂O₃). Basa yang tidak bereaksi kemudian dapat didaur ulang, mengurangi konsumsi bahan kimia. Pada Tahap 2, kalium titanat yang dihasilkan kemudian dilindi dengan asam klorida (HCl) untuk melarutkan titanium. Inovasi kunci dari proses ini terletak pada Stage 3, dimana Ethylenediaminetetraacetic acid (EDTA) digunakan sebagai agen pengkelat selama hidrolisis. EDTA secara selektif mengikat ion besi (Fe³⁺) untuk membentuk kompleks Fe-EDTA yang stabil, sehingga memisahkan dan menghilangkan pengotor besi dari larutan titanium. Teknik pemurnian ini telah terbukti menghasilkan titanium dioksida dengan kemurnian yang sangat tinggi, mencapai 99% (Wang et al., 2007; Xiong et al., 2013).
Dekomposisi Alkali (NaOH/KOH)
Metode ini menawarkan alternatif yang menarik. Alih-alih menggunakan asam pekat, struktur ilmenit dihancurkan dengan larutan NaOH atau KOH pekat. Reaksi ini menghasilkan intermediate titanat yang kemudian dapat dihidrolisis dengan asam untuk mendapatkan TiO₂. Sebuah studi melaporkan bahwa metode ini berhasil mengekstrak 98% titanium dari ilmenit dengan kemurnian produk di atas 99% (Sampath et al., 2023). Keunggulannya jelas yaitu menghindari penggunaan asam pekat sejak awal. Tantangannya adalah biaya daur ulang larutan alkali yang tinggi.
Reduksi Magnesiothermic (dengan Magnesium)
Metode ini secara cepat dapat mengubah ilmenit langsung menjadi berbagai paduan titanium yang sangat berharga, seperti FeTi (paduan besi-titanium) dan TiC (titanium karbida). Ilmenit dicampur dengan logam magnesium dan dipanaskan pada suhu tinggi dalam atmosfer inert. Hasil pembakaran kemudian dicuci dengan asam untuk memisahkan paduan titanium dari produk sampingnya. Metode ini mampu menghasilkan bubuk paduan dengan kemurnian lebih dari 95% (Sampath et al., 2023), membuka pintu untuk aplikasi material maju.
Electro-reduction dalam Garam Lelehan
Metode ini dianggap canggih karena menggunakan listrik untuk mereduksi langsung ilmenit menjadi paduan titanium di dalam wadah berisi garam lelehan (seperti CaCl₂). Metode ini fleksibel dan dapat “diprogram” untuk menghasilkan berbagai paduan dan komposit seperti Ti₅Si₃ dan Fe/TiC, tergantung pada komposisi bahan awal (Sampath et al., 2023).
Masa Depan Pengolahan Ilmenit
Perjalanan pengolahan ilmenit adalah cerita tentang evolusi dan inovasi. Dari proses sulfat yang sarat limbah hingga metode dekomposisi alkali yang lebih ramah lingkungan, dan dari produksi TiO₂ tunggal hingga sintesis berbagai paduan canggih, tujuannya tetap sama : memaksimalkan nilai tambah sambil meminimalkan jejak ekologis. Tantangan ke depan adalah menyempurnakan metode-metode baru ini agar lebih ekonomis, efisien, dan benar-benar berkelanjutan. Dengan kekayaan ilmenit yang dimiliki Indonesia, eksplorasi dan adaptasi metode-metode ini bukan hanya sebuah pilihan, melainkan sebuah keharusan untuk mengubah potensi geologis menjadi keunggulan industri yang nyata
Daftar Referensi:
Anbia, M., Ahmadian, F., Rezaie, M., 2018. Preparation of titanium dioxide nanostructure from ilmenite through sulfate-leaching process and solvent extraction by D2EHPA. J. Iran. Chem. Soc. 15, 2533–2540. https://doi.org/10.1007/s13738-018- 1441-9.
Hart, J.R., 2011. Ethylenediaminetetraacetic Acid and Related Chelating Agents, in: Ullmann’s Encyclopedia of Industrial Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany. https://doi.org/10.1002/14356007.a10_095.pub2.
Sampath, A.H.J., Wickramasinghe, N.D., de Silva, K.M.N., & de Silva, R.M, 2023. Methods of Extracting TiO₂ and Other Related Compounds from Ilmenite. Minerals, *13*(5), 662. https://doi.org/10.1016/j.hydromet.2020.105507
Xiong, X., Wang, Z., Wu, F., Li, X., Guo, H., 2013. Preparation of TiO2 from ilmenite using sulfuric acid decomposition of the titania residue combined with separation of Fe3+ with EDTA during hydrolysis. Adv. Powder Technol. 24, 60–67. https://doi.org/10.1016/J.APT.2012.02.002.









