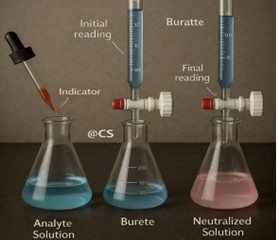
Titrasi adalah salah satu teknik analisis kimia kuantitatif yang paling mendasar dan sering digunakan di laboratorium. Prinsip utama titrasi adalah metode volumetri, di mana kita mengukur volume suatu larutan yang konsentrasinya sudah diketahui (titran) untuk menentukan konsentrasi larutan lain yang tidak diketahui (analit). Proses ini didasarkan pada reaksi kimia yang stoikiometrinya (perbandingan mol) sudah diketahui secara pasti.
Inti dari titrasi adalah mencapai titik ekuivalen, yaitu titik di mana jumlah mol titran yang ditambahkan sama persis dengan jumlah mol analit dalam sampel, sesuai dengan perbandingan reaksi. Untuk mengamati titik ini, kita biasanya menggunakan indikator yang mengalami perubahan warna signifikan. Perubahan warna yang teramati ini disebut titik akhir titrasi, yang idealnya harus sangat dekat dengan titik ekuivalen.
Jenis-Jenis Titrasi Berdasarkan Reaksi Kimia
Metode titrasi dikategorikan berdasarkan jenis reaksi kimia yang terjadi antara titran dan analit. Setiap jenis memiliki karakteristik dan aplikasi spesifik.
- Titrasi Asam-Basa
Titrasi ini didasarkan pada reaksi netralisasi antara asam dan basa.
- Titran: Larutan standar asam atau basa kuat.
- Analit: Larutan basa atau asam yang konsentrasinya tidak diketahui.
- Indikator: Indikator pH, seperti fenolftalein (berubah dari tak berwarna menjadi merah muda pada suasana basa) atau metil jingga (berubah dari merah menjadi kuning pada suasana basa).
Contoh: Menentukan konsentrasi asam asetat dalam cuka dengan titrasi menggunakan larutan standar natrium hidroksida (NaOH).
- Titrasi Redoks (Reduksi-Oksidasi)
Titrasi ini melibatkan transfer elektron antara titran dan analit. Reaksi ini digunakan untuk menentukan konsentrasi zat-zat yang dapat teroksidasi atau tereduksi.
- Titran: Oksidator atau reduktor kuat, seperti kalium permanganat (KMnO4) atau kalium dikromat (K2Cr2O7).
- Analit: Zat yang dapat mengalami reaksi redoks.
- Indikator: Dapat menggunakan autoindikator (misalnya KMnO4 yang berwarna ungu) atau indikator redoks eksternal.
Contoh: Menentukan konsentrasi ion besi (Fe2+) dalam sampel dengan titrasi menggunakan kalium permanganat (KMnO4).
- Titrasi Kompleksometri
Titrasi ini didasarkan pada pembentukan senyawa kompleks yang stabil dan larut antara titran dan analit. Agen pengompleks yang paling umum adalah EDTA (asam etilendiamintetraasetat).
- Titran: Larutan standar EDTA.
- Analit: Ion logam, seperti Ca2+, Mg2+, atau Zn2+.
- Indikator: Indikator yang dapat membentuk kompleks berwarna dengan ion logam.
Contoh: Menentukan kesadahan air (konsentrasi ion Ca2+ dan Mg2+) menggunakan titrasi EDTA.
- Titrasi Pengendapan
Titrasi ini melibatkan pembentukan endapan yang sangat tidak larut antara titran dan analit.
- Titran: Larutan standar perak nitrat (AgNO3).
- Analit: Ion halida, seperti klorida (Cl−) atau bromida (Br−).
- Indikator: Biasanya menggunakan indikator, seperti kromat, yang membentuk endapan berwarna.
Contoh: Menentukan konsentrasi klorida (Cl−) dalam air limbah dengan titrasi menggunakan perak nitrat (AgNO3), dikenal juga sebagai metode Mohr.
Setiap jenis titrasi memiliki aplikasinya sendiri dalam berbagai bidang, mulai dari analisis farmasi hingga kontrol kualitas makanan. Dengan pemahaman yang baik tentang prinsip dan jenis-jenisnya, titrasi tetap menjadi alat yang sangat kuat dan akurat di tangan seorang analis kimia.