Metalurgi kromium adalah teknologi metalurgi untuk mengekstraksi senyawa kromium, kromium logam, dan paduan dari bahan yang mengandung kromium. Pada tahun 1797, N.-L. Vauquelin pertama kali menemukan elemen ini dari bijih timbal halofil merah Siberia (krokoit PbCrO4). Nama Inggris untuk kromium berasal dari bahasa Yunani “chroma,” yang berarti “warna,” karena senyawa kromium memiliki warna yang berbeda. Kandungan kromium dalam kerak bumi adalah 0,006–0,035%, yang termasuk salah satu elemen yang tersebar luas. Mineral yang mengandung kromium dengan nilai pemanfaatan industri adalah mineral spinel kromium, dan rumus umum kimianya adalah (Fe,Mg)(Cr,A1,Fe)2O4 atau (Fe,Mg)O⋅(Cr,Al,Fe)2O3, di mana kandungan kromium oksida (Cr2O3) adalah 18–62%. Mineral spinel kromium terutama meliputi kromit (FeCr2O4), kromit magnesian [(Fe,Mg)Cr2O4], alumokromit [Fe(Cr,Al)2O4], dan mineral spinel kaya kromium [(Fe,Mg)(Cr,Al)2O4]. Karena beberapa besi atau kromium dalam kromit digantikan oleh homeomorfisme seperti magnesium atau aluminium, mineral spinel kromium dengan kandungan kromium tinggi secara umum disebut sebagai kromit dalam peleburan aktual (Shaojun and Kuangdi, 2023).
Kromit dikenal sebagai mineral logam yang tahan terhadap korosi akibat pembentukan pasivasi pada permukaan logam. Passivasi adalah suatu kondisi yang disertai dengan pembentukan lapisan oksida pasif yang sangat tahan terhadap asam pada permukaannya, sehingga mengurangi korosi secara signifikan. Hal ini terjadi akibat dari pembentukan lapisan pelindung pada permukaan logam (Moslehifard et al., 2020). Kromit biasanya diaplikasikan untuk produksi pembuatan baja tahan karat dan paduan logam yang mengandung kromium seperti baja tahan karat ferro – kromium (Sanchez-Segado, Escudero-Castejón and Jha, 2025), paduan Co-Cr-Mo dengan paduan berbasis Ni-Cr (Moslehifard et al., 2020), dan produk utama dari pembuatan garam kromium seperti natrium dikromat (Na2Cr2O7) (Shaojun and Kuangdi, 2023).
Berbagai metode diterapkan dalam recovery kromium di antaranya melalui metode peleburan bijih kromit dalam suasana reduksi di tungku busur terendam dengan kokas pada suhu di atas 1600 °C. Namun, metode ini mengonsumsi energi dari 3000 hingga 4200 kWh per ton. Dalam peleburan busur terendam, suhu dan potensi oksigen dikontrol dengan cermat untuk menghindari pembentukan karbida kompleks dan hilangnya sub-oksida kromium (CrO) dalam fase gas. Pengendalian karbon terlarut dalam paduan Fe-Cr cair dan padat sangat penting untuk meminimalkan pengendapan karbida biner dan terner yang kompleks. Dengan tujuan mengurangi konsumsi energi yang tinggi dari proses peleburan, reduksi keadaan padat parsial kromit ditunjukkan dalam tungku putar pada suhu antara 1200 °C hingga 1400 °C, sebelum peleburan. Namun, proses ini memiliki keterbatasannya sendiri, seperti suhu tinggi yang diperlukan dan kinetika lambat dari proses reduksi kromium (Sanchez-Segado, Escudero-Castejón and Jha, 2025).
Berbagai proses lainnya diterapkan untuk menghindari konsumsi energi yang besar seperti proses oksidasi pemanggangan natrium karbonat (soda-ash/Na2CO3), metode pemanggangan kalsium, metode pemanggangan tanpa kalsium (Shaojun and Kuangdi, 2023), pelindian asam, pelindian alkali, dan peleburan alkali telah dikembangkan untuk pengolahan bijih kromit guna menghasilkan natrium kromat (Na2CrO4) dan natrium dikromat (Na2Cr2O7), yang merupakan produk utama yang digunakan untuk pembuatan berbagai bahan kimia kromium. Karena alasan ekonomi dan teknis, hanya pemanggangan natrium karbonat yang telah digunakan secara komersial di seluruh dunia, baik di tungku putar (rotary furnace) maupun di tungku perapian putar (rotary hearth furnace) (Sanchez-Segado, Escudero-Castejón and Jha, 2025).
Le Chatelier, pada abad ke-19, pertama kali menerapkan pemanggangan alkali dalam kondisi pengoksidasi untuk ekstraksi natrium kromat dari bijih kromit. Penemuan ini menjadi dasar bagi proses industri yang masih dipraktikkan hingga saat ini. Penerapan proses pemanggangan alkali untuk ekstraksi oksida logam yang berbeda, seperti Ti, Nb, Ta, unsur tanah jarang, Al atau V, dari mineral kompleks juga telah diselidiki dengan hasil yang memuaskan. Pemanggangan alkali kromit untuk menghasilkan natrium kromat (Na2CrO4) dilakukan dengan adanya oksigen atau udara didasarkan pada oksidasi ion Cr3+ menjadi ion Cr6+ dalam mineral pada kisaran suhu 1000–1200 °C, yang mengarah pada pembentukan kromat yang larut dalam air. Bahan yang dipanggang kemudian dicuci dengan air untuk secara selektif melarutkan natrium kromat. Padatan tidak larut yang tersisa, yang dikenal sebagai residu pengolahan bijih kromit (COPR), terutama mengandung oksida besi, oksida magnesium, silikat yang tidak larut, dan kromit yang tidak bereaksi (Sanchez-Segado, Escudero-Castejón and Jha, 2025).
Prinsip dan alur proses pemanggangan natrium karbonat untuk menghasilkan garam/natrium dikromat (Na2Cr2O7) dapat ditunjukkan pada gambar di bawah ini:
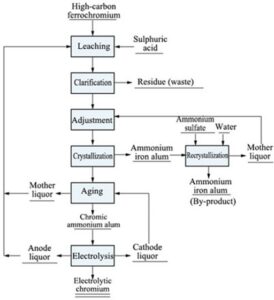
Proses Produksi natirum dikromat adalah sebagai berikut: setelah penggilingan mineral yang mengandung kromit, natrium karbonat (Na2CO3) dilakukan pemanggangan oksidasi pada suhu 950–1250 ºC untuk mendapatkan klinker pemanggangan oksidasi kromit. Klinker tersebut dicuci dengan air secara arus balik dan disaring untuk mendapatkan larutan yang mengandung natrium kromit. Kemudian, asam sulfat ditambahkan untuk menyesuaikan nilai pH larutan natrium kromat, dan pengotor yang mengandung aluminium yang terlarut dalam larutan diendapkan dan dihilangkan dalam bentuk aluminium hidroksida. Setelah netralisasi dan penghilangan aluminium, vanadium dihilangkan dari larutan dan kemudian diasamkan dengan asam sulfat untuk mendapatkan larutan natrium dikromat. Ketika larutan pekat diuapkan hingga sekitar 1100 g/L yang mengandung Na2Cr2O7⋅2H2O, kristal natrium sulfat didinginkan dan disaring, dan kemudian larutan dipekatkan hingga 1500–1550 g/L yang mengandung natrium dikromat, suhunya dijaga pada 90–100 ºC selama 8 jam, dan kemudian natrium dikromat didinginkan dan dikristalkan (Shaojun and Kuangdi, 2023).
Beberapa riset PT Global Mineralium Corporindo dalam memperoleh kromit dari bijih yang mengandung chrome tinggi dengan kadar platinum (Pt) yang tinggi di dalamnya, dengan tujuan menghilangkan kromit yang tahan terhadap asam menjadi bijih yang bebas kromit untuk proses refining metalurgi platinum adalah melalui reduksi oksidatif menggunakan Na2CO3. Mekanisme prosesnya adalah:
1. Bijih yang mengandung kromium dan PGM dalam jumlah tinggi dihancurkan hingga menjadi partikel halus. Proses ini bertujuan untuk meningkatkan luas permukaan bijih, sehingga reaksi dengan natrium karbonat (Na2CO3) dapat berjalan lebih efisien. Setelah dihancurkan, bijih dicampur secara homogen dengan bubuk natrium karbonat.



2. Campuran bijih dan natrium karbonat kemudian dipanaskan dalam tanur hingga suhu tinggi yang telah ditentukan suhunya. Pada suhu ini, campuran akan mengalami proses peleburan atau sintering, di mana butiran-butiran partikel bijih dan natrium karbonat menyatu. Dalam kondisi panas ini, natrium karbonat akan bereaksi dengan oksida kromium dalam bijih.


3. Dengan adanya udara (oksigen). Pada suhu ini, bijih yang mengandung kromium akan bereaksi dengan natrium karbonat dan oksigen, menghasilkan natrium kromat (Na2Cr2O4) yang berwarna kuning dan oksida besi (Fe2O3). Reaksi ini mengoksidasi kromium dari keadaan oksidasi +3 menjadi +6. Reaksi kimianya adalah:
4FeCr2O4 + 8Na2CO3 + 7O2 → 8Na2CrO4 + 2Fe2O3 + 8CO2
4. Setelah proses pemanggangan, padatan yang dihasilkan, yang merupakan campuran natrium kromat dan oksida besi, didinginkan. Campuran ini kemudian dilarutkan dalam air panas pada suhu 80-90°C. Pada suhu ini, natrium kromat (Na2CrO4) akan larut sepenuhnya dalam air, membentuk larutan berwarna kuning. Sebaliknya, oksida besi (Fe2O3) dan kotoran lainnya tidak larut. Larutan yang telah dihasilkan, yang mengandung natrium kromat terlarut, kemudian disaring untuk memisahkan padatan yang tidak larut (oksida besi dan kotoran lainnya) dari larutan. Hasil penyaringan adalah larutan murni natrium kromat.


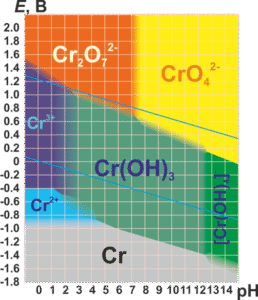
Sesuai dengan diagram Pourbaix Cr, warna larutan hasil pencucian bijih rosting berwarna kuning menandakan Cr terlarut menjadi garam kromat membentuk Cr2O42-.
5. Larutan ini selanjutnya dapat diolah lebih lanjut untuk menghasilkan berbagai garam kromium lainnya, seperti natrium dikromat (Na2Cr2O7). Proses ini dilakukan dengan menambahkan asam (seperti asam sulfat) ke dalam larutan natrium kromat, mengubahnya menjadi dikromat.
2Na2Cr2O4 + H2SO4 → Na2Cr2O7 + Na2SO4 + H2O
Selanjutnya, natrium dikromat dapat direduksi lebih lanjut untuk menghasilkan kromium trioksida (Cr2O3) atau bahkan logam kromium murni.
6. Terakhir akan meninggalkan residu yang tidak larut yang di dalamnya mengandung oksida besi dan logam PGM dengan konsentrasi kromium yang telah direduksi konsentrasinya untuk masuk ke pemurnian lebih lanjut.
Moslehifard, E. et al. (2020) ‘Effect of chemical passivation on corrosion behavior and ion release of a commercial chromium-cobalt alloy’, Journal of Dental Research, Dental Clinics, Dental Prospects, 14(3), pp. 171–176. Available at: https://doi.org/10.34172/joddd.2020.037.
Sanchez-Segado, S., Escudero-Castejón, L. and Jha, A. (2025) ‘Kinetics analysis and Cr(6+)-free reaction mechanism of the alkali reduction of South African chromite ores for Cr2O3 extraction’, Minerals Engineering, 232(October 2024). Available at: https://doi.org/10.1016/j.mineng.2025.109595.
Shaojun, C. and Kuangdi, X. (2023) (Springer Nature Reference) Kuangdi Xu (editor) – The ECPH Encyclopedia of Mining and Metallurgy, The ECPH Encyclopedia of Mining and Metallurgy. Available at: https://doi.org/10.1007/978-981-19-0740-1_963-1.
Zhu, F.X. and Qi, W.F. (2007) ‘1-error linear complexity of pn-periodic sequences over Fp’, Dianzi Yu Xinxi Xuebao/Journal of Electronics and Information Technology, 29(9), pp. 2222–2225.









